

Nonostante le apparenze, questo esercizio è tutt'altro che difficile. Nel modello corpuscolare dell'atomo di idrogeno, l'energia potenziale del sistema formato da un elettrone che ruota attorno al nucleo a distanza r da esso è pari a:
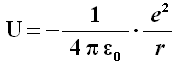
Se l'elettrone si trova in una sferetta di raggio r, la sua quantità di moto p non può essere inferiore all’incertezza data dal Principio di Indeterminazione di Heisenberg:
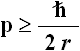
Quindi anche l'energia cinetica Ec dell'elettrone ha un limite inferiore, dato da:
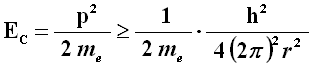
Il raggio r è quello per cui queste due energie sono circa uguali in valore assoluto. Uguagliando U ed Ec troviamo così:
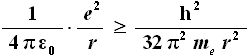
Da cui si ottiene:
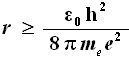
Sostituendo in essa i valori numerici abbiamo:
![]()
La risposta esatta è dunque la numero 4 (le altre contengono al denominatore diverse potenze di 2). Si osservi che la formula appena ricavata coincide con la (3.4) in cui si ponga n = 1, cioè con il raggio della prima orbita elettronica calcolato nel modello di Bohr! Anche in questo caso, tutto va perfettamente al suo posto.

Werner Heisenberg e Niels Bohr fanno colazione insieme nel 1934
